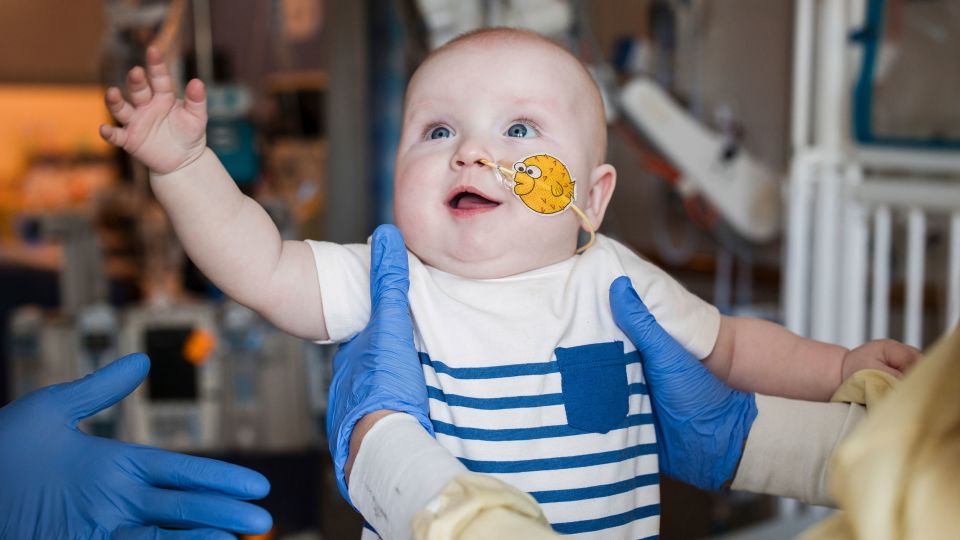
طفل مولود مصاب بمرض وراثي نادر وخطير ينمو ويزدهر بعد الحصول على علاج تجريبي لتحرير الجينات.
وصف الباحثون القضية في دراسة جديدة ، قائلين إنه من بين أول من عولجوا بنجاح مع علاج مخصص يسعى إلى إصلاح خطأ صغير ولكنه حاسم في رمزه الوراثي الذي يقتل نصف الرضع المصابين. على الرغم من أن ذلك قد يمر بعض الوقت قبل أن تتوفر علاجات مخصصة مماثلة للآخرين ، يأمل الأطباء في أن تساعد التكنولوجيا يومًا ما الملايين الخلفين حتى مع تقدم الطب الوراثي لأن ظروفهم نادرة جدًا.
“هذه هي الخطوة الأولى نحو استخدام علاجات تحرير الجينات لعلاج مجموعة واسعة من الاضطرابات الوراثية النادرة التي لا توجد حاليًا علاجات طبية نهائية”.
الطفل ، KJ Muldoon من Clifton Heights ، بنسلفانيا ، هو واحد من 350 مليون شخص في جميع أنحاء العالم مع أمراض نادرة ، معظمها وراثي. تم تشخيصه بعد فترة وجيزة من الولادة بنقص CPS1 الشديد ، الذي يقدره بعض الخبراء للتأثير على واحد من بين كل مليون طفل. يفتقر هؤلاء الرضع إلى إنزيم مطلوب للمساعدة في إزالة الأمونيا من الجسم ، بحيث يمكن أن يتراكم في دمهم ويصبح سامًا. زرع الكبد هو خيار للبعض.
مع العلم أن احتمالات KJ ، والآباء Kyle و Nicole Muldoon ، وكلاهما 34 ، قلقين من فقدانه.
وقالت نيكول: “كنا ، كما تعلمون ، نزن جميع الخيارات ، وطرح جميع الأسئلة إما لعملية زرع الكبد ، وهو أمر غازي ، أو شيء لم يتم القيام به من قبل”.
وأضاف زوجها: “لقد صلينا ، تحدثنا إلى الناس ، وجمعنا المعلومات ، وقررنا في النهاية أن هذه هي الطريقة التي سنذهب بها”.
يجلس KJ Muldoon ، في الوسط ، مع أشقائه بعد جرعة متابعة من علاج تحرير الجينات التجريبية في أبريل. (كلو داوسون/مستشفى الأطفال في فيلادلفيا عبر AP) – كلوي داوسون/مستشفى الأطفال في فيلادلفيا/AP
في غضون ستة أشهر ، ابتكر الفريق في مستشفى الأطفال في فيلادلفيا وبنس ، إلى جانب شركائهم ، علاجًا مصممًا لتصحيح جين KJ المعيب. لقد استخدموا CRISPR ، أداة تحرير الجينات التي فازت بمخترعها بجائزة نوبل في عام 2020. بدلاً من قطع حبلا الحمض النووي مثل مقاربات كريسبر الأولى ، استخدم الأطباء تقنية تقلب الحمض النووي المتحور “رسالة” – المعروفة أيضًا باسم القاعدة – إلى النوع الصحيح. المعروف باسم “التحرير الأساسي” ، فهو يقلل من خطر التغيرات الوراثية غير المقصودة.
وقال باحث العلاج الجيني في مستشفى سانت جود للأطفال في ممفيس ، الذي لم يشارك في الدراسة ، إنه “من المثير للغاية” أن قام الفريق بإنشاء العلاج بهذه السرعة. “هذا يحدد حقًا السرعة والمعيار لمثل هذه الأساليب.”
في فبراير ، حصل KJ على أول ضخه الرابع مع علاج تحرير الجينات ، الذي تم تسليمه من خلال قطرات دهنية صغيرة تسمى الجسيمات النانوية الدهنية التي يتم تناولها بواسطة خلايا الكبد.
بينما كانت الغرفة مغرمة بالإثارة في ذلك اليوم ، “لقد نام من خلال كل شيء” ، يتذكر مؤلف الدراسة الدكتورة ريبيكا أهرينز ، خبير في العلاج الجيني في Chop.
بعد جرعات المتابعة في مارس وأبريل ، تمكنت KJ من تناول الطعام بشكل طبيعي وتعافى جيدًا من أمراض مثل نزلات البرد ، والتي يمكن أن تؤثر على الجسم وتزيد من أعراض CPS1. يبلغ عمر 9 أشهر أيضًا أدوية أقل.
وقال والدته: “في أي وقت نرى فيه أصغر معلم يلتقي به – مثل موجة صغيرة أو يتدحرج – هذه لحظة كبيرة بالنسبة لنا”.
ومع ذلك ، حذر الباحثون من أن الأمر لم يكن سوى بضعة أشهر. سيحتاجون إلى مشاهدته لسنوات.
“ما زلنا في المراحل المبكرة من فهم ما قد يفعله هذا الدواء من أجل KJ” ، قال Ahrens-Nicklas. “لكن كل يوم ، يظهر لنا علامات على أنه ينمو ويزدهر”.

يجلس KJ Muldoon مع والديه ، Kyle و Nicole Muldoon ، وإخوته في أبريل. – كلو داوسون/مستشفى الأطفال في فيلادلفيا/AP
يأمل الباحثون أن ما يتعلمونه من KJ سيساعد مرضى الأمراض النادرة الآخرين.
تستهدف العلاجات الجينية ، التي يمكن أن تكون مكلفة للغاية تطويرها ، الاضطرابات الأكثر شيوعًا بشكل عام لأسباب مالية بسيطة: المزيد من المرضى يعنيون المزيد من المبيعات ، مما قد يساعد في دفع تكاليف التطوير وتوليد المزيد من الأرباح. على سبيل المثال ، يعالج علاج كريسبر الأول الذي وافق عليه إدارة الغذاء والدواء الأمريكية ، على سبيل المثال ، مرض الخلايا المنجلية ، وهو اضطراب في الدم المؤلم الذي يؤثر على الملايين في جميع أنحاء العالم.
وقال موسونورو إن عمل فريقه – الذي تموله المعاهد الوطنية للصحة جزئياً – أظهر أن إنشاء علاج مخصص لا يجب أن يكون مكلفًا للغاية. وقال إن التكلفة “لم تكن بعيدة” عن 800000 دولار زائد لزرع الكبد المتوسط والرعاية ذات الصلة.
وقالت موسونورو: “نظرًا لأننا نتحسن وأفضل في صنع هذه العلاجات ونقصر الإطار الزمني أكثر ، فإن اقتصادات الحجم ستدخل وأتوقع أن تنخفض التكاليف”.
وقال بووبالان إن العلماء لن يضطروا أيضًا إلى إعادة جميع الأعمال الأولية في كل مرة يقومون فيها بإنشاء علاج مخصص ، لذا فإن هذا البحث “يمهد المرحلة” لعلاج الظروف النادرة الأخرى.
وقال كارلوس موريس ، أستاذ الأعصاب في جامعة ميامي الذي لم يشارك في الدراسة ، إن الأبحاث مثل هذا يفتح الباب لمزيد من التقدم.
وقال: “بمجرد أن يأتي شخص ما مع تقدم مثل هذا ، لن يستغرق الأمر وقتًا” لفرق أخرى لتطبيق الدروس والمضي قدمًا. “هناك حواجز ، لكنني أتوقع أن يتم عبورها في السنوات الخمس إلى العشر القادمة. ثم سيتحرك الحقل بأكمله ككتلة لأننا مستعدون إلى حد كبير.”
لمزيد من الأخبار والنشرات الإخبارية CNN قم بإنشاء حساب في CNN.com
















اترك ردك